ग्रासनली (ईसोफेगस)
ग्रासनली (ईसोफेगस) शरीर में एक ट्यूब जैसी संरचना है जो मुंह को पेट से जोड़ती है. यह लगभग 25 सेमी लंबी होती है और अंदर से बाहर तक चार परतों से बनी होती है, श्लेष्मा, उप-श्लेष्मा, मांसपेशियों की परत और बाहरी परत जिसे एडिटिटिया कहा जाता है. भोजन जो मुंह में निगला जाता है, ग्रासनली (ईसोफेगस) के माध्यम से पेट तक पहुंचता है. ईसोफेगस में मांसपेशी परत इसके माध्यम से भोजन को आगे बढ़ाने में मदद करती है. जंक्शन जहां ग्रासनली (ईसोफेगस) समाप्त होती है, और पेट शुरू होता है, उसे ईसोफेगो-गैस्ट्रिक जंक्शन के रूप में जाना जाता है.
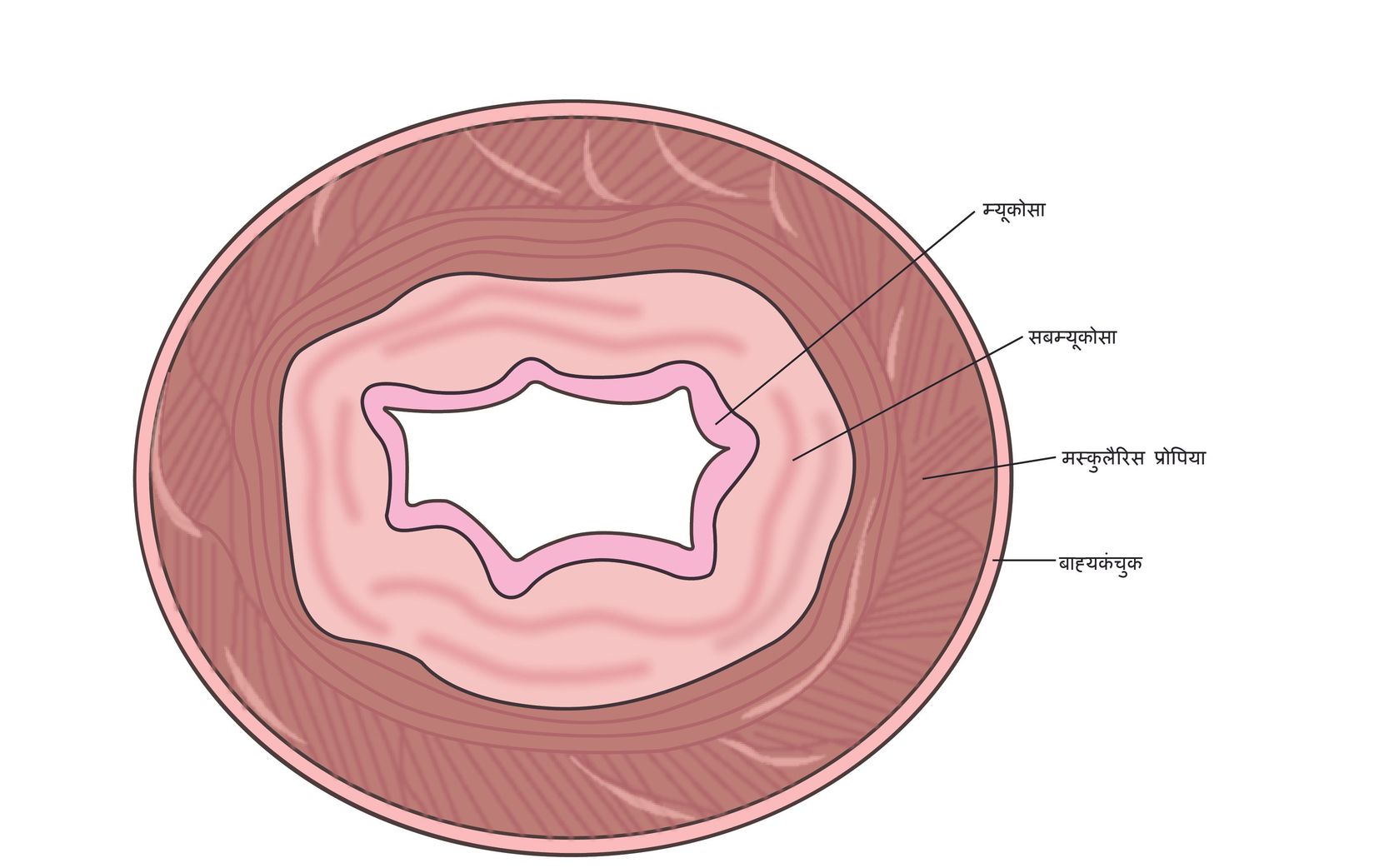

ग्रसिका कैंसर
ग्रसिका (इेसोफेजियल) कैंसर वह कैंसर होता है जो ग्रासनली (ईसोफेगस) में शुरू हुआ है. यह कैंसर आमतौर पर श्लेष्मा (म्यूकोसा) में उत्पन्न होता है जो ट्यूब की अंदरूनी परत है. इसोफेजियल कैंसर एक स्क्वैमस सेल कार्सिनोमा या एडेनोकार्सिनोमा हो सकता है. श्लैष्मिक सेल कार्सिनोमा श्लेष्मा को अस्तर करने वाली कोशिकाओं से उत्पन्न होता है. एडेनोकार्सिनोमा ग्रंथि कोशिकाओं से उत्पन्न होता है जो ग्रासनली (ईसोफेगस) में श्लेष्मा का उत्पादन करता है. ये दोनों कैंसर 95% से अधिक ईसोफेजियल कैंसर होते हैं.
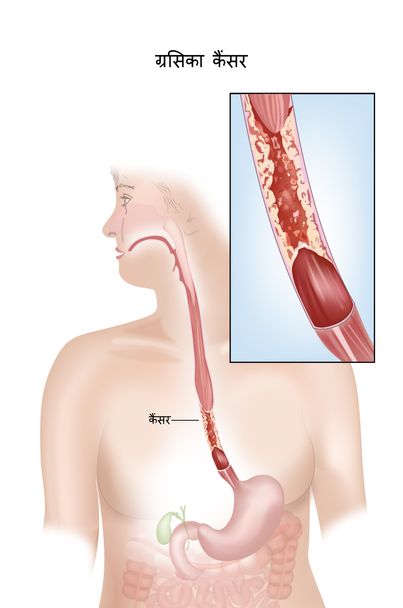
ईसोफेजियल कैंसर से जुड़े विभिन्न जोखिम कारक हैं. ये जोखिम कारक पट्टकी कोशिका (स्क्वैमस सेल) और एडेनोकार्सिनोमा के लिए अलग हो सकते हैं. कुछ जोखिम कारक दोनों प्रकार के लिए सामान्य हैं.
धूम्रपान और शराब
स्क्वैमस सेल प्रकार के कैंसर के विकास में धूम्रपान और शराब महत्वपूर्ण भूमिका निभाते हैं. सिगरेट धूम्रपान में सिगार धूम्रपान से अधिक जोखिम की संभावना होती है. खपत की गई शराब के वास्तविक प्रकार की तुलना में खपत की गई शराब की कुल मात्रा मुख्य निर्धारक होती है.
आहार
नाइट्रोसो यौगिकों में उच्च आहार का जोखिम अधिक होता हैं. कच्चे खाद्य पदार्थ जिन्हें सुखाया जाता है, अचार बनाया जाता है या धूम्रित किया जाता है, उनमें नाइट्रोसो यौगिक होते हैं.
सुपारी चबाने से खतरा बढ़ जाता है. बहुत गर्म पेय का सेवन (जैसे बहुत गर्म चाय) करने से ईसोफेजियल लाइनिंग में ऊष्मा क्षति उत्पन्न होने से जोखिम बढ़ जाता है.
पूर्व ईसोफेजियल स्थितियां
पिछली या अंतर्निहित ईसोफेगल स्थितियां जैसे कि अचलासिया कार्डिया, ईसोफेगल सख्ती या एट्रोफिक गैस्ट्रेटिस होने से जोखिम बढ़ जाता है.
मोटापा
अधिक वजन या मोटापे के कारण गैस्टो-इसोफेजियल प्रतिवाह होने लगता है. आम तौर पर पेट और ईसोफेगस के जंक्शन को बहुत कसकर बंद कर दिया जाता है और पेट से ईसोफेगस में एसिड के गुजरने से रोकता है. मोटे मरीजों में, जंक्शन शिथिल हो जाता है और एसिड को ईसोफेगस में गुजरने की अनुमति देता है. इसे प्रतिवाह रोग कहा जाता है और इससे बैरेट के ईसोफेगस नामक स्थिति का विकास हो सकता है. इससे ईसोफेगस के एडेनोकार्सिनोमा का विकास हो सकता है.
बैरेट का ईसोफेगस
बैरेट का ईसोफेगस एक ऐसी स्थिति है जहां पेट से एसिड के लगातार संपर्क में रहने के कारण ईसोफेगस के निचले सिरे की अंदरूनी परत एक प्रकार से दूसरे प्रकार में बदल जाती है. बैरेट के ईसोफेगस होने से ईसोफेजियल कैंसर के विकास का खतरा बढ़ जाता है.
टाइलोसिस
टाइलोसिस विरासत में मिली त्वचा की स्थिति का एक दुर्लभ रूप है. इससे ग्रसित लोगों में ग्रसिका कैंसर होने का खतरा बढ़ जाता है.
ग्रसिका (ईसोफेलियल) कैंसर कई लक्षण पैदा कर सकता है. इनमें से कोई भी लक्षण होने का मतलब यह नहीं है कि कैंसर है, लेकिन लक्षणों की जांच के लिए डॉक्टर के पास जाना जरूरी है. इसोफेगस के एडेनोकार्सिनोमा और स्क्वैमस सेल कार्सिनोमा उसी तरह से मौजूद होते हैं.
निगलने में कठिनाई
यह ग्रसिका (ईसोफेलियल) कैंसर वाले लोगों के लिए एक आम लक्षण है. निगलने में कठिनाई शुरू में ठोस और फिर तरल पदार्थ के लिए हो सकती है. लक्षण आमतौर पर प्रगतिशील होते हैं और वजन कम करने से जुड़े हो सकते हैं. मरीज देख सकते हैं कि जब कठिनाई शुरू होती है, तो इसे शुरू में पानी की घूंट लेने से दूर किया जा सकता है.
उल्टी या भोजन का पुन: उमड़ाव
कुछ लोग नोटिस करते हैं कि पहले खाये गये भोजन की उल्टी हो गई है या मुंह में फिर से उमड़ाव हो गया है. भोजन के फिर से उमड़ाव का मतलब है कि निगल लिया गया भोजन पेट में प्रवेश किए बिना मुंह में वापस आ जाता है. यह भोजन को निगलने के बाद पेट में नहीं जाने के कारण होता है.
निगलने में दर्द
निगलने पर दर्द ग्रसिका (ईसोफेलियल) कैंसर की उपस्थिति का एक लक्षण और संकेत हो सकता है. दर्द गले के क्षेत्र में या छाती की हड्डी के पीछे छाती में हो सकता है.
हृद्दाह के लगातार लक्षण
हृद्दाह सामान्य जन में एक सामान्य लक्षण है और मुख्य रूप से गैर-कैंसर स्थितियों के कारण होता है. लेकिन जिन लोगों को लगातार हृद्दाह या अपच होता है, उन्हें अपने डॉक्टर के पास जाना चाहिए क्योंकि यह एक ग्रसिका (ईसोफेलियल) कैंसर की उपस्थिति के कारण हो सकता है.
कफ या आवाज में परिवर्तन
आवाज की खराबी और खांसी ग्रसिका (ईसोफेलियल) कैंसर के लक्षण हो सकते हैं.
अन्य लक्षण
अन्य लक्षण जो ग्रसिका (ईसोफेलियल) कैंसर में मौजूद हो सकते हैं, उनमें खून की उल्टी, वजन में कमी या पेट में दर्द, थकावट और पेट में सूजन शामिल हैं.
जब ग्रासनल (ईसोफेलियल) कैंसर का संदेह होता है या निदान किया जाता है, तो निम्नलिखित जांच की जाती है:
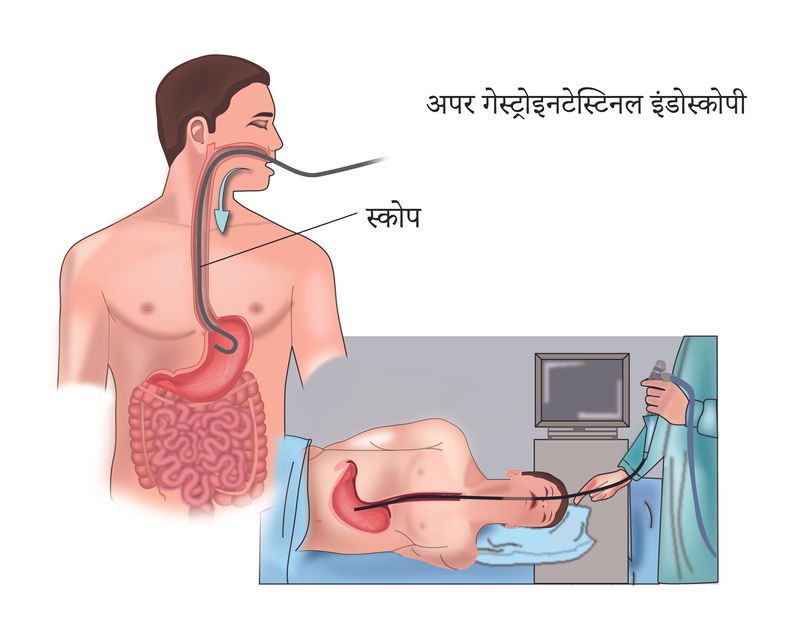
ऊपरी जीआई एंडोस्कोपी
यह एक परीक्षण है जिसमें असामान्यता देखने के लिए ईसोफेगस और पेट में एक पतली ट्यूब को गुजारना शामिल है. ट्यूब में एक प्रकाश और इसके अंत में एक कैमरा होता है ताकि प्रक्रिया करने वाले डॉक्टर ईसोफेगस और पेट को देख सकें. परीक्षण हल्के बेहोश करने की क्रिया का उपयोग करके किया जाता है और दर्द रहित होता है.
यह एक दिन की प्रक्रिया है, इसलिए मरीज को अस्पताल में रात भर रहने की जरूरत नहीं है. यदि डॉक्टर एंडोस्कोपी पर एक असामान्य क्षेत्र देखता है, तो उसी समय एक बायोप्सी किया जा सकता है.
सीटी स्कैन
एक बार जब ग्रासनली (ईसोफेलियल) कैंसर का निदान एंडोस्कोपी पर किया जाता है तो सीटी या कंप्यूटेड टोमोग्राफिक स्कैन किया जाता है. सीटी स्कैन शरीर के अंदर की विस्तृत छवियों को प्राप्त करने के लिए एक्स-रे का उपयोग करता है.
इसलिए, यह इस बारे में जानकारी दे सकता है कि कैंसर शरीर के अन्य भागों में फैल गया है या नहीं.
पीईटी स्कैन या पीईटी-सीटी स्कैन
पीईटी-सीटी स्कैन एक विशेष सीटी स्कैन है जहां सीटी स्कैन से पहले रेडियोधर्मी अनुरेखक (ट्रैसर) को शरीर में इंजेक्ट किया जाता है. यह अनुरेखक शरीर के भीतर उन क्षेत्रों में रहता है जहां ग्लूकोज की उच्च आवश्यकता होती है. चूंकि कैंसर को जीवित रहने के लिए बहुत अधिक ग्लूकोज की आवश्यकता होती है, वे शरीर के बाकी हिस्सों की तुलना में बहुत अधिक ट्रैसर को लेते हैं. तब कैंसर को स्कैन पर आसानी से देखा जा सकता है. पीईटी-सीटी स्कैन कैंसर के प्रसार के साक्ष्य के लिए मानक सीटी स्कैन की तुलना में अधिक संवेदनशील है. उपचार से पहले ग्रासनली (ईसोफेलियल) कैंसर के चरण में यह एक बहुत महत्वपूर्ण परीक्षण है.
एंडोस्कोपिक अल्ट्रासाउंड (ईयूएस)
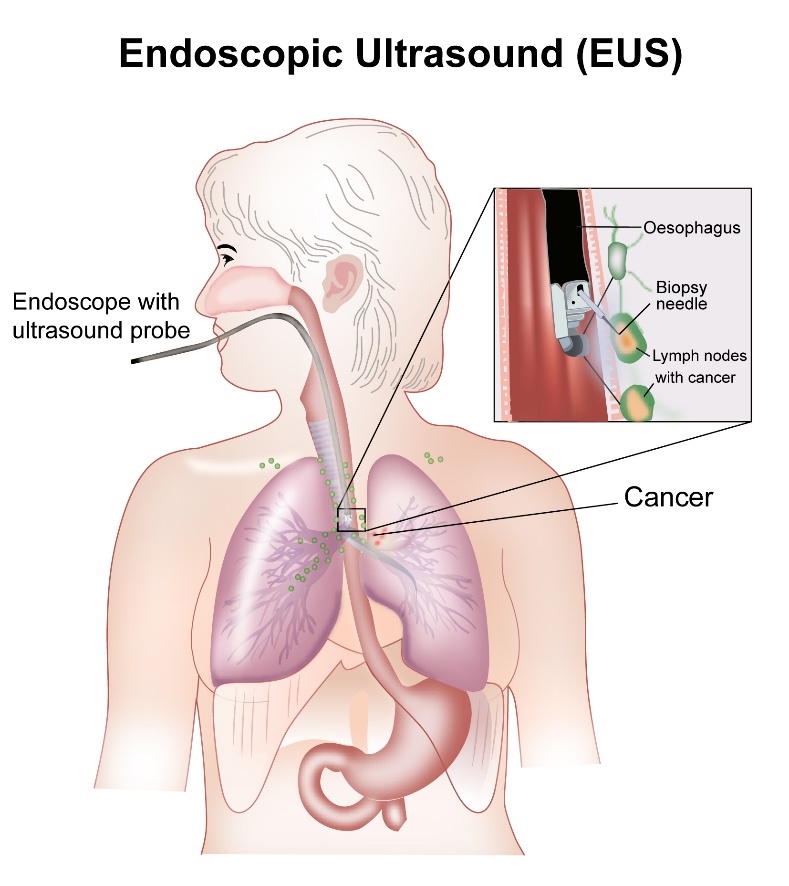
एंडोस्कोपिक अल्ट्रासाउंड एक परीक्षण है जो एंडोस्कोपीबुट की तरह होता है और इसके अंत में एक अल्ट्रासाउंड स्कैनर होता है. यह परीक्षण ईसोफेगस की दीवारों में कैंसर के प्रसार की गहराई को देखने के लिए ध्वनि तरंगों का उपयोग करता है. स्कैनर कैंसर के आसपास मौजूद किसी भी बढ़े हुए लिम्फ नोड्स को देखने में मदद करता है. परीक्षण का उपयोग कैंसर के सटीक चरण का पता लगाने और किसी भी असामान्य पर्व (नोड्स) की बायोप्सी करने में मदद करने के लिए किया जाता है.
लेप्रोस्कोपी
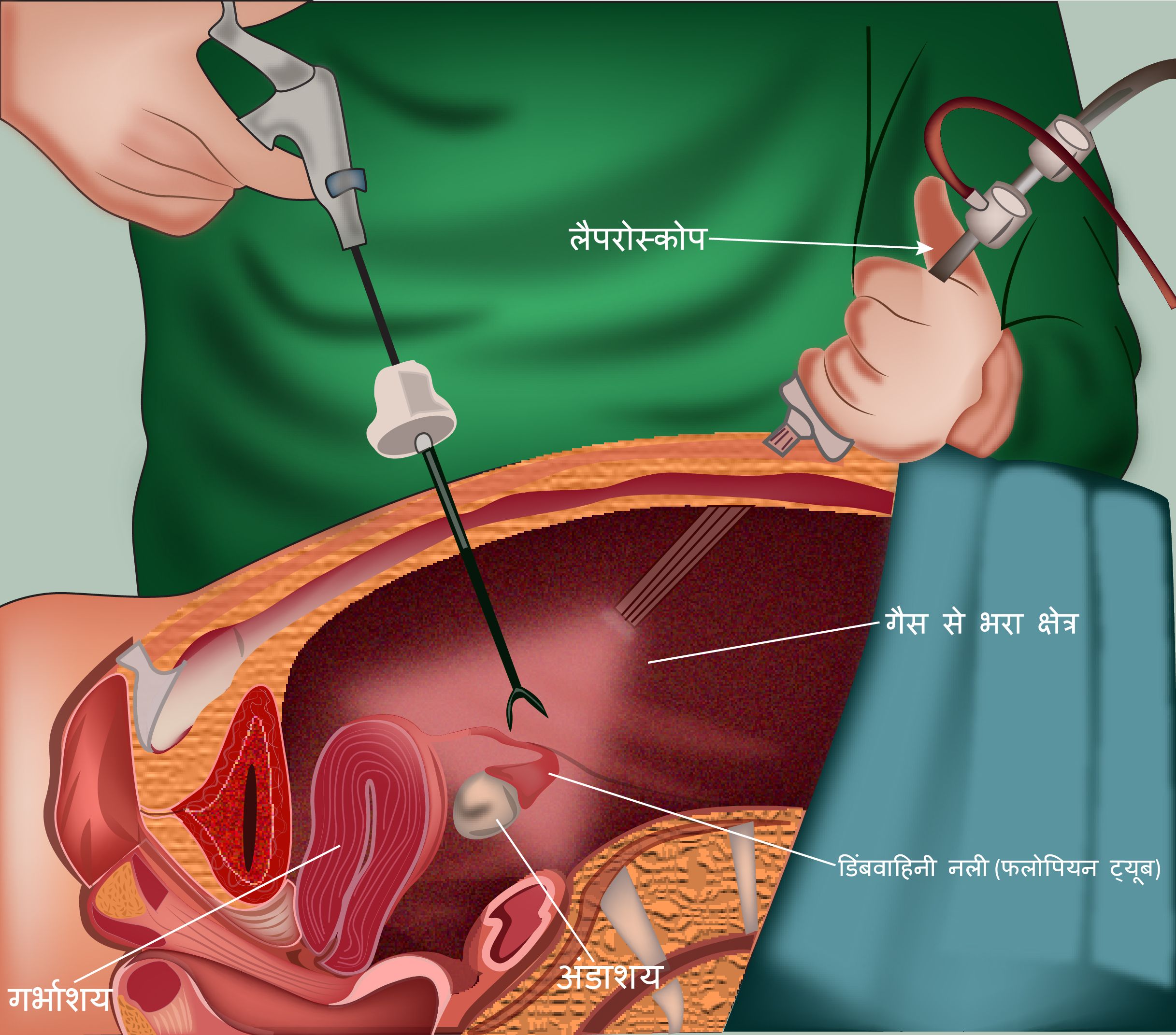
लेप्रोस्कोपी एक परीक्षण होता है जो डॉक्टर को पेट के अंदर देखने में मदद करता है. यह परीक्षण पेट में कैंसर के फैलाव का पता लगाने के लिए ग्रासनली (ईसोफेलियल) कैंसर से पीड़ित कुछ मरीजों में किया जाता है.
परीक्षण सामान्य एनेस्थेसिया के तहत किया जाता है और मरीज को अस्पताल में कम रहने की आवश्यकता होगी.
इसमें एक छोटा चीरा शामिल होता है, जो नाभि के चारों ओर एक इंच आकार का होता है. एक लेप्रोस्कोप चीरा के माध्यम से पारित किया जाता है और डॉक्टर अंदर देख सकते हैं. जरूरत पड़ने पर बायोप्सी ली जा सकती है. प्रक्रिया के दौरान कार्बन डाइऑक्साइड गैस पेट में पारित हो जाती है ताकि अंदर बेहतर दृश्य प्राप्त करने में मदद मिल सके. यह कार्बन डाइऑक्साइड गैस कुछ समय के बाद समाप्त हो जाएगी.
टीएनएम अवस्था (स्टेजिंग) या नंबर स्टेजिंग के आधार पर ईसोफेजियल कैंसर की अवस्था का निर्धारण किया जाता है. ये दो अवस्था निर्धारण प्रणालियां (स्टेजिंग सिस्टम) नीचे दी गई हैं:
ईसोफेजियल कैंसर की टीएनएम स्टेजिंग
टीएनएम का अर्थ है ट्यूमर, नोड और मेटास्टेस
टी स्टेजिंग
T का अर्थ ट्यूमर का आकार है. T को T1 से T4 में विभाजित किया गया है. इस कैंसर में टी स्टेजिंग ट्यूमर द्वारा ईसोफेजियल दीवार के प्रसार की गहराई पर आधारित है.
| T1 | ट्यूमर लामिना प्रोप्रिया या उप-श्लेष्मा पर आक्रमण करता है |
| T2 | ट्यूमर ईसोफैगस की मांसपेशी परत पर आक्रमण करता है |
| T3 | ट्यूमर ईसोफैगस की बाहरी परत (एडेविटिया) पर हमला करता है |
| T4 | ट्यूमर ईसोफेगस को पार करता है और ईसोफेगस के आसपास अन्य संरचनाओं पर हमला करता है |
एन स्टेजिंग
एन स्टेजिंग ईसोफेगस के चारों ओर लिम्फ नोड्स के समावेशन पर निर्भर करेगा.
| Nx | लिम्फ नोड के समावेशन का आकलन नहीं किया जा सकता है. |
| N0 | कैंसर द्वारा लिम्फ नोड्स का कोई समावेशन नहीं. |
| एन1 | कैंसर द्वारा 1-2 लिम्फ नोड्स का समावेश |
| एन2 | कैंसर द्वारा 3-6 लिम्फ नोड्स का समावेश |
| एन3 | कैंसर द्वारा 7 या अधिक लिम्फ नोड्स का समावेश |
एम स्टेजिंग
एम स्टेजिंग से शरीर के सुदूर हिस्सों तक कैंसर फैलने की जानकारी मिलती है .
| M0 | कैंसर के दूर तक फैलने का कोई सबूत नहीं |
| M1 | कैंसर के दूर तक फैलने की उपस्थिति |
नंबर स्टेजिंग
इस प्रकार का स्टेजिंग टीएनएम वर्गीकरण के आधार पर अवस्था 1 से 4 तक के कैंसर की अवस्था बताता है. ग्रासिका कैंसर में यह स्टेजिंग सिस्टम स्क्वैमस सेल कैंसर और एडेनोकार्सिनोमा प्रकार के लिए अलग-अलग है. एडेनोकार्सिनोमा नीचे दर्शाया गया है.
एडेनोकार्सिनोमा के लिए नंबर स्टेजिंग
- T1 N0 M0————स्टेज 1
- T1 N1 M0————स्टेज 2A
- T2 N0 M0————स्टेज 2B
- T2 N1 M0————स्टेज 3
- T2 N0-1 M0———स्टेज 3
- T4a N0-1 M0——-स्टेज 3
- T1-4a N2 M0——-स्टेज 4a
- T4b N0-2 M0——-स्टेज 4a
- Any T N3 M0——-स्टेज 4a
- Any T Any N M1—स्टेज 4b
कैंसर का ग्रेड
कैंसर की ग्रेडिंग इस बात पर आधारित होती है कि कोशिकाएं माइक्रोस्कोप के तहत कैसी दिखाई देती हैं. कुछ कैंसर में ग्रेडिंग 1 से 3 या 4 तक हो सकती है. ग्रेड 1 सामान्य कोशिकाओं की तरह दिखने वाली कोशिकाएं और ग्रेड 4 ऐसी कोशिकाएं हैं जो सामान्य कोशिकाओं से बिल्कुल नहीं मिलती हैं.
ईसोफेजियल कैंसर के ग्रेड
ग्रेड 1- कैंसर में कोशिकाएँ अच्छी तरह से विभेदित होती हैं (सामान्य कोशिकाओं की तरह दिखती हैं)
ग्रेड 2- कैंसर में कोशिकाओं को मध्यम रूप से विभेदित होती हैं.
ग्रेड 3-कैंसर में कोशिकाएँ विकृत रूप से भिन्न होती हैं (सामान्य कोशिकाओं के समान नहीं होती)
ग्रेड 4-कोशिकाएं समरूप होती हैं (पूरी तरह से अलग दिखती हैं)
ग्रासनली (ईसोफेजियल) कैंसर का इलाज सर्जरी, कीमोथेरेपी, रेडियोथेरेपी या इन विधियों के संयोजन से किया जा सकता है. उपचार का सटीक तरीका निदान में कैंसर की अवस्था और मरीज की सामान्य शारीरिक स्थिति पर निर्भर करता है.
प्रारंभिक ग्रासनली (ईसोफेजियल) कैंसर में, उपचार का उद्देश्य मरीज को उपचार के साथ ठीक करना होगा.
उन्नत कैंसर (अवस्था 4 या भारी अवस्था 3) में, इलाज संभव हो सकता है या नहीं भी हो सकता है, लेकिन कैंसर को कम करने और इसे नियंत्रित करने के लिए उपचार दिया जाता है.
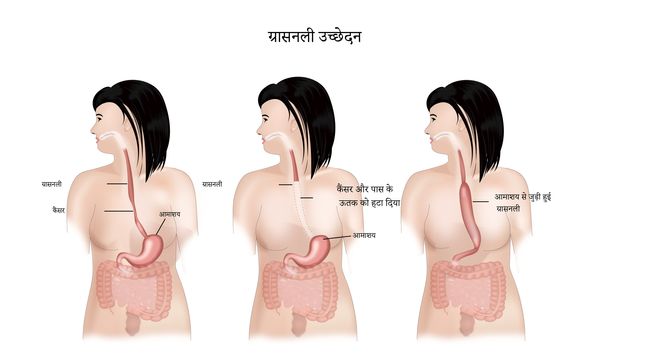
ग्रासनली (ईसोफेजियल) कैंसर का सर्जिकल निष्कासन (पृथक्करण) ईसोफजियल कैंसर के उपचार का एक आम और महत्वपूर्ण घटक है. ईसोफेगस को निकालने को ग्रासनलीउच्छेदन कहा जाता है.
ग्रासनली उच्छेदन स्टेल 1, 2 और 3 ईसोफेजियल (स्क्वैमस सेल या एडेनोकार्सिनोमा) कैंसर के प्रबंधन में एक विकल्प है. यह स्टेज 4 कैंसर के प्रबंधन में एक विकल्प नहीं है.
ग्रासनली उच्छेदन में कैंसर वाले ईसोफेगस के खंड को बाहर निकालना और शेष अनुभागों को एक साथ जोड़ना शामिल है. शेष ईसोफेगस को जोड़ने के लिए पेट को आमतौर पर छाती में खींच लिया जाता है. कभी-कभी दो कट अनुभागों को एक साथ जोड़ने के लिए बृहदान्त्र (बड़ी आंत) के एक हिस्से की आवश्यकता हो सकती है. यदि कैंसर निचले ईसोफेगस में या ईसोफेगस और पेट के जंक्शन पर है, तो कैंसर के आसपास पर्याप्त मार्जिन प्राप्त करने के लिए पेट के एक हिस्से को भी हटा दिया जाता है. ऑपरेशन के दौरान, सर्जन ईसोफेगस के आसपास मौजूद लिम्फ ग्रंथियों को भी हटा देगा.
ऑपरेशन के समय, एक फीडिंग ट्यूब लगायी जा सकती है ताकि सर्जरी से उबरने के दौरान मरीज को वह सभी पोषण मिल सके जिसकी उसे जरूरत है. यह फीडिंग ट्यूब एक फीडिंग जेन्जोस्टॉमी हो सकती है जहां ट्यूब को छोटी आंत में रखा जाता है जिसे जेजुनम या गैस्ट्रोस्टोमी कहा जाता है, जहां ट्यूब पेट में होती है. ये नलिकाएं त्वचा से बाहर निकलती हैं और भोजन और तरल पदार्थ ट्यूब के माध्यम से अंदर धकेल दिए जाते हैं.
सर्जरी के प्रकार
सर्जरी तीन तरीकों से की जा सकती है-
- ट्रान्स-थोरैसिक ग्रासनलीउच्छेदन (ट्रांस-थोरैसिक ऑसोफेगेटॉमी)– जहां चीरों को छाती और पेट पर लगाया जाता है
- ट्रान्स-हायटल ग्रासनलीउच्छेदन (ट्रांस-हायटल ऑसोफेगेटॉमी)– जहां गर्दन और पेट में चीरे लगाए जाते हैं
- त्रि-चीरीय ग्रासनलीउच्छेदन – चीरा गर्दन, छाती और पेट में लगाया जाता है .
सभी तीन तरीके समान रूप से प्रभावी हैं, और विधि का चुनाव कैंसर के स्थान और सर्जन के अनुभव पर निर्भर करता है.
कुछ लोग कीहोल सर्जरी का उपयोग करके ऑपरेशन करने में सक्षम हो सकते हैं. यह छाती में एक थोरैकोस्कोप और पेट में लेप्रोस्कोप का उपयोग करके किया जाता है.
ऑपरेशन योग्य स्टेज 1 के ईसोफेजियल कैंसर (स्क्वैमस सेल या एडेनोकार्सिनोमा) के लिए, अपने आप पर शल्य चिकित्सा से निकालने का विकल्प है, बशर्ते मरीज ऑपरेशन करने के लिए पर्याप्त रूप से फिट हो.
ऑपरेशन योग्य स्टेज 2 और 3 के मरीजों के लिए, सर्जरी द्वारा निकालने से पहले कीमोथेरेपी अथवा कीमोथेरेपी और रेडियोथेरेपी (कीमोरेडियोथेरेपी) के संयोजन पर चिचार किया जाता है. किस विकल्प का इस्तेमाल किया जाए, यह वस्तुत: मरीज के फिटनेस स्तर पर निर्भर करेगा.
सर्जरी के बाद, अधिकांश रोगी गहन देखभाल में कुछ दिन बिताएंगे और फिर उन्हें वार्ड में स्थानांतरित किया जाएगा. सामान्य रूप से खाने पर वापस आने में समय लगेगा और खाने की आदतें आमतौर पर ऑपरेशन से पहले अलग होंगी. इसका कारण ऑपरेशन के बाद ग्रास नली (गुलेट) और पेट के आकार और आकार में परिवर्तन है. मरीज को दिन में अधिक बार थोड़े-थोड़े भोजन करने पड़ सकते हैं. साथ ही, एसिड प्रतिवाह और डायरिया के लक्षणों को नियंत्रित करने के लिए मरीज को एंटासिड और डायरिया रोधी गोलियां लेनी पड़ सकती हैं.
ईसोफेगल और पेट की सर्जरी के बाद एक अनुषंगी प्रभाव डंपिंग सिंड्रोम है. यह खाना खाने के बाद बेहोश होने की अनुभूति है. इस प्रकार की सर्जरी के बाद यह एक सामान्य घटना है और इसे धीरे-धीरे खाने से, आहार में बहुत अधिक शक्कर सामग्री को कम करने और थोड़े-थोड़े आहारों को अधिक बार खाने से कम किया जा सकता है;
कीमोथेरेपी
कीमोथेरेपी इंजेक्शन, ड्रिप और टैबलेट के रूप में दी जाने वाली कैंसर प्रतिरोधी दवाओं का उपयोग है. ये दवाएं कैंसर कोशिकाओं को अधिकतम नुकसान और साथ ही सामान्य ऊतकों को कुछ नुकसान पहुंचा करके कैंसर कोशिकाओं को मारने में मदद करती हैं. कीमोथेरेपी के परिणामस्वरूप होने वाले अनुषंगी प्रभाव सामान्य ऊतकों पर इन दवाओं के प्रभाव के कारण होते हैं. कैंसर का इलाज करने के लिए कई कीमोथेरेपी दवाओं का उपयोग किया जाता है. इन दवाओं का उपयोग या तो संयोजन में या एकल एजेंट के रूप में किया जा सकता है. कीमोथेरेपी को चक्र के रूप में दिया जाता है, प्रत्येक चक्र 1 से 4 सप्ताह के बीच होता है, आमतौर पर 3 सप्ताह का होता है. दो कीमोथेरेपी चक्रों के बीच अंतर शरीर को अगले डोज से पहले ठीक करने के लिए है. कीमोथेरेपी का कोर्स आमतौर पर कुछ महीनों तक चलता है.
ग्रासनली कैंसर में कीमोथेरेपी
कीमोथेरपी ग्रासनली कैंसर के उपचार के लिए एक महत्वपूर्ण घटक है. केमोथेरेपी को ग्रासनली कैंसर में विभिन्न सेटिंग्स में दिया जाता है.
स्टेज 1, 2 और 3 कैन्सर में रेडियोथेरेपी के साथ-साथ कीमोथेरेपी दी जा सकती है. इस विकल्प को समवर्ती कीमोरेडियोथेरेपी कहा जाता है. इसे सप्ताह में एक बार या हर तीन सप्ताह में एक बार या रेडियोथेरेपी के पहले और आखिरी सप्ताह में दिया जा सकता है. सबसे अच्छी रणनीति कीमोथेरेपी को सहन करने की मरीज की क्षमता और मरीज की सुविधा पर निर्भर करेगी.
कुछ सेटिंग्स में, कीमोथेरेपी को ग्रासनली कैंसर के सर्जरी से निकालने से पहले दिया जा सकता है. इसे नियोज्वुवेंट कीमोथेरेपी कहा जाता है. कीमोथेरेपी कभी कभी सर्जरी से निकालने के बाद दिया जा सकता है. इसे सहयोगी कीमोथेरेपी कहा जाता है.
स्टेज 4 कैंसर में, कीमोथेरेपी का उपयोग कैंसर को नियंत्रित करने और कैंसर से उत्पन्न होने वाले लक्षणों को नियंत्रित करने के लिए एक संयोजन उपचार के रूप में किया जाता है. स्टेज 2 और 3 में कीमोथेरेपी का उद्देश्य मरीज को कैंसर से ठीक करना है और स्टेज 4 में कैंसर को नियंत्रित करना और दीर्घायु बनाना है.
ग्रासनली कैंसर में आमतौर पर इस्तेमाल की जाने वाली कीमोथेरेपी दवाओं में एपिरुबिसिन, डॉक्सोरूबिसिन, 5 फ्लूरोरासिल (5 एफयू), कैपेसिटाबाइन, सिस्प्लैटिन या कार्बोप्लाटिन, ऑक्सिप्लिप्टिन, इरिनोटेकन, डोसेटेक्सेल, पैक्लिटैक्सेल और ट्रैस्टुज़ुमाब शामिल हैं. जब इन दवाओं का संयोजन के रूप में उपयोग किया जाता है, तो सामान्य संयोजन होते हैं:
DCF (डोसेटेक्सेल, सिस्प्लैटिन और 5FU)
ECF (एपीरुबिसिन, सिस्प्लैटिन, 5 एफयू)
ECX (एपीरुबिसिन, सिस्प्लैटिन, कैपेसिटाबाइन)
EOX (एपिरूबिसिन, ऑक्सिप्लिप्टिन, कैपेसिटाबाइन)
FOLFOX (ऑक्सिप्लिपटिन और 5FU)
XELOX (ऑक्सिप्लिप्टिन और कैपेसिटाबाइन)
सिस्प्लैटिन और 5FU
एचईआर2 परीक्षण और ट्रैस्टुजुमैब
एचईआर2 एक बाहृय त्वचीय विकास कारक रिसेप्टर 2 है, जो कि जब ईसोफैगोगैस्ट्रिक कैंसर में बढ़ जाता है तो कैंसर बढ़ सकता है. सभी ईसोफेगो- गैस्ट्रिक कैंसर के 35% तक एचईआर2 पॉजिटिव होते हैं और कैंसर के निदान के लिए इसका हमेशा परीक्षण किया जाना चाहिए. एचईआर2 स्थिति का परीक्षण उस कैंसर नमूने पर किया जाता है जो बायोप्सी या सर्जरी के समय मिलता है. यह परीक्षण बताएगा कि 3 + का परिणाम देकर कैंसर में हर 2 को प्रवर्धित किया जाता है या बढ़ाया जाता है या नहीं. प्रारंभिक एचईआर 2 परीक्षण संदिग्ध (2+) है, जब एक और परीक्षण की आवश्यकता होती है.
यदि एचईआर2 परीक्षण पॉजिटिव है, तो एचईआर2 रिसेप्टर के खिलाफ एंटीबॉडी उपलब्ध हैं और इस प्रकार के कैंसर के उपचार के रूप में उपयोग किया जाता है.
ट्रैस्टुजुमैब एचईआर2 रिसेप्टर के लिए एक एंटीबॉडी है और इस दवा का उपयोग एचईआर2 पॉजिटिव मरीजों में कीमोथेरेपी के साथ करने से अतिरिक्त लाभ होता है. यह दवा केवल स्टेज 4 मरीजों में कीमोथेरेपी के साथ प्रयोग की जाती है.
कीमोथेरेपी के अनुषंगी प्रभाव
ग्रासनली कैंसर के लिए कीमोथेरेपी अनुषंगी प्रभावों (साइड इफेक्ट) के साथ जुड़ा हुआ है. ये उन दवाओं पर निर्भर करते हैं जो प्रशासित हैं. इनमें से कुछ अनुषंगी प्रभावों को दवाओं से अच्छी तरह से नियंत्रित किया जा सकता है. कीमोथेरेपी की सहनशीलता एक व्यक्ति से दूसरे व्यक्ति में भिन्न होती है. कुछ लोग बिना किसी साइड इफ़ेक्ट के बहुत अच्छी तरह से उपचार का सामना करते हैं, जबकि अन्य को साइड इफ़ेक्ट हो सकते हैं. आम अनुषंगी प्रभाव हैं-
बालों का झड़ना
यह उपर्युक्त कीमोथेरेपी रेजिमेंस के साथ आम बात है. बालों का झड़ना आमतौर पर पहले चक्र के दूसरे सप्ताह के बाद शुरू होता है. कीमोथेरेपी समाप्त होने के बाद बाल वापस उगते हैं. कुछ केंद्र एक “कोल्ड कैप” सेवा प्रदान कर सकते हैं जो बालों के झड़ने की संभावना को कम कर सकती है.
मचली और उल्टी
यह कीमोथेरेपी का एक ज्ञात अनुषंगी प्रभाव है, लेकिन आधुनिक दवाओं के साथ, ये लक्षण बहुत अच्छी तरह से नियंत्रित होते हैं.
थकान
थकान एक आम अनुषंगी प्रभाव है. यह आमतौर पर पहले सप्ताह में अधिक होता है और फिर उसके बाद धीरे-धीरे सुधार होता है.
मुंह में छाले
कीमोथेरेपी के बाद आम बात है. यह अपने आप व्यवस्थित हो जाएगा और मुंह को साफ रखने के लिए दिन में 3-4 बार माउथ वॉश का उपयोग करने की सिफारिश की जाती है.
पतली टट्टी
यह लक्षण कभी-कभी कीमोथेरेपी के बाद हो सकता है. अपने चिकित्सक से संपर्क करें. यदि ऐसा होता है तो दवाओं से इसे अच्छी तरह से नियंत्रित किया जा सकता है.
कब्ज़
कब्ज कीमोथेरेपी का एक आम अनुषंगी प्रभाव है. यह स्वयं कीमोथेरेपी दवा के परिणामस्वरूप हो सकता है, लेकिन मुख्य रूप से यह मतली रोधी दवाओं के प्रभाव के कारण होता है जो कि कीमोथेरेपी के साथ दी जाती हैं. कीमोथेरेपी के पहले कुछ दिनों में कब्ज पैदा होता है.
संक्रमण का जोखिम
यह कीमोथेरेपी का एक महत्वपूर्ण अनुषंगी प्रभाव है. ऐसा होता है क्योंकि कीमोथेरेपी संक्रमण से लड़ने के लिए शरीर की क्षमता को कम करती है. इसलिए, कीमोथेरेपी के दौरान किसी भी समय (भले ही वह आधी रात में हो) बुखार होने पर तत्काल डॉक्टर से संपर्क करना बहुत महत्वपूर्ण है.
स्वाद में परिवर्तन
यह कीमोथेरेपी के साथ आम है और इसलिए पहले की तरह भोजन स्वादिष्ट नहीं लगेगा. कीमोथेरेपी समाप्त होने के बाद स्वाद ठीक हो जाएगा.
हाथ-पैर में झुनझुनी
कुछ कीमोथेरेपी दवाएं यह अनुषंगी प्रभाव उत्पन्न करती हैं. अपने अगले विजिट में इसे उन्हें डॉक्टर को बताएं.
अरक्तता
यह कीमोथेरेपी के परिणामस्वरूप हो सकता है. आमतौर पर यह सिर्फ देखा जा सकता है और उपचार खत्म होने के बाद इसमें सुधार होगा. इसे सुधारने के लिए कभी-कभी रक्त आधान या अन्य उपचार आवश्यक होता है.
रक्तस्राव
कीमोथेरेपी के साथ रक्तस्राव का यह एक छोटा जोखिम है. यदि ऐसा होता है, तो आपको अपने डॉक्टर से सीधे संपर्क करने की आवश्यकता है.
खांसी, श्वासहीनता या पैरों में सूजन
ये प्रभाव ट्रैस्टुजुमैबैंड वाले मरीजों में हो सकते हैं .अगर ऐसा होता है तो डॉक्टर को सूचित किया जाना चाहिए.
रेडियोथेरेपी क्या है
रेडियोथेरेपी कैंसर कोशिकाओं को मारने के लिए दी जाने वाली उच्च ऊर्जा एक्स-रे का उपयोग है. ये एक्स-रे कैंसर कोशिकाओं के डीएनए को क्षति पहुंचाते हैं और इस तरह उन्हें मार देते हैं. रेडियोथेरेपी एक स्थानीय उपचार है और इसका प्रभाव उस क्षेत्र पर पड़ता है जहां इसे दिया जाता है. यह एक बड़ी मशीन (रैखिक त्वरक) का उपयोग करके दिया जाता है जो एक्स-रे उत्पन्न करता है और मरीज को उपचार प्रदान करता है. इस विधि को बाह्य किरण चिकित्सा कहा जाता है. रेडियोथेरेपी देने का दूसरा तरीका रेडियोएक्टिव स्रोतों को कैंसर में डालना है. इस विधि को ब्रेकीथेरेपी कहा जाता है और इसका उपयोग कुछ प्रकार के ग्रासनली कैंसरों के इलाज के लिए किया जाता है.
ग्रासनली कैंसर के लिए रेडियोथेरेपी
रेडियोथेरेपी ग्रासनली कैंसर के लिए उपचार का एक महत्वपूर्ण घटक है. इसका उपयोग ग्रासनली कैंसर (स्टेज 1 से 4) के सभी अवस्थाओं का इलाज करने के लिए किया जाता है. स्टेज 1, 2 और 3 में, रेडियोथेरेपी का उपयोग एक उपचारात्मक इरादे के साथ किया जाता है जिसका अर्थ है कि भविष्य में वापस आने के बिना कैंसर से पूरी तरह से छुटकारा पाना है. ऐसी परिस्थितियों में, उपचार पांच से सात सप्ताह के लिए प्रतिदिन, सप्ताह में पांच दिन दिया जाता है.
स्टेज 1 ग्रासनली कैंसर में, रेडियोथेरेपी का उपयोग उन मरीजों में किया जाता है जो सर्जरी के लिए फिट नहीं हैं. उस सेटिंग में, रेडियोथेरेपी कीमोथेरेपी के साथ या मरीज की फिटनेस के आधार पर दी जाती है.
स्टेज 2 और 3 के मरीजों में, केमोरेडियोथेरेपी या रेडियोथेरेपी को या तो उपचार के रूप में दिया जाता है या मरीज की फिटनेस के आधार पर फिर से उपचारात्मक सर्जरी से पहले दिया जाता है.
स्टेज 4 में, रेडियोथेरेपी का उपयोग मुख्य रूप से लक्षणों को नियंत्रित करने के लिए किया जाता है. यहां, इसे 1 से 3 सप्ताह तक की छोटी अवधि में दिया जाता है. ब्रैकीथेरेपी का उपयोग स्टेज 4 के रोगियों में भी किया जा सकता है. इसमें स्थानीय स्तर पर विकिरण देने के लिए एक संक्षिप्त अवधि के लिए ग्रासनली में एक रेडियोधर्मी स्रोत डालना शामिल है. इस उपचार को अपने दम पर इस्तेमाल किया जा सकता है या बाहरी बीम रेडियोथेरेपी के साथ जोड़ा जा सकता है.
जब कीमोरेडियोथेरेपी का उपयोग किया जाता है, तो इस्तेमाल की जाने वाली दवाओं के आधार पर कीमोथेरेपी दो चरणों में दी जाती है. आमतौर पर, यह हर सप्ताह में एक बार कीमोथेरेपी के रूप में होता है या उपचार के पहले और अंतिम सप्ताह में 5 दिनों तक लगातार होता है.
रेडियोथेरेपी विभिन्न तकनीकों का उपयोग करके दी जा सकती है और इन्हें नीचे सूचीबद्ध किया गया है.
3डी कन्फर्मल रेडियोथेरेपी
यह रेडियोथेरेपी की योजना बनाने और देने का एक तरीका है, जहां ट्यूमर की त्रि-आयामी छवि प्राप्त करने के लिए सीटी, एमआरआई स्कैन का उपयोग किया जाता है. इससे नियोजन प्रक्रिया को तीन आयामों में बनाया जा सकता है;
इसमें मानक 2 डी रेडियोथेरेपी की तुलना में विकिरण उपचार के अधिक सटीक होने की गुंजाइश होती है.
इंटेंसिटी मॉड्यूलेटेड रेडियोथेरेपी (आईएमआरटी)
आईएमआरटी एक प्रकार की 3डी अनुरूप उपचार योजना और वितरण विधि है, जहां विकिरण बीम को ट्यूमर के आकार को ठीक करने के लिए आकार दिया जा सकता है. यह शरीर में आसपास की सामान्य संरचनाओं में विषाक्तता को कम करने में मदद करता है. आईएमआरटी और 3D कन्फर्मल रेडियोथेरेपी के बीच अंतर यह है कि आईएमआरटी ट्यूमर के आकार को फिट करने के लिए अधिक सटीक रूप से आकार ले सकता है. इसलिए, अनुषंगी प्रभाव कम होंगे. इसके अलावा, आईएमआरटी के साथ, एक ही ट्यूमर के विभिन्न हिस्सों में रेडियोथेरेपी की विभिन्न खुराक देने की संभावना है. आईएमआरटी विभिन्न कोणों से ट्यूमर पर निर्देशित कई विकिरण किरणों का उपयोग करके किया जाता है.
आर्क आधारित उपचार
आर्क आधारित थेरेपी (रैपिड आर्क, वीएमएटी) रेडियोथेरेपी की डिलीवरी है, जिसमें रैखिक त्वरक एक चाप जैसे रूप में मरीज के चारों ओर घूम रहा है. इस प्रकार की थेरेपी मानक आईएमआरटी से अधिक सटीक और डिलीवरी करने में तेज हो सकती है. यह अधिक महंगा भी है.
इमेज गाइडेड रेडियोथेरेपी (आईजीआरटी)
इमेज गाइडेड रेडियोथेरेपी उपचार सटीकता की निगरानी के लिए सीटी स्कैनर जैसे इमेजिंग सिस्टम का उपयोग है. आम तौर पर, मानक 3 डी अनुरूप रेडियोथेरेपी में, नियोजन उद्देश्यों के लिए उपचार शुरू करने से पहले एक सीटी स्कैन किया जाता है. आईजीआरटी में, उपचार की सटीकता के लिए परीक्षण करने के लिए प्रत्येक रेडियोथेरेपी उपचार से पहले एक सीटी स्कैन या एक्स-रे कराया जा सकता है.
ग्रासनली पर रेडियोथेरेपी का अनुषंगी प्रभाव
ग्रासनली के लिए रेडियोथेरेपी से जुड़े अनुषंगी प्रभाव (साइड इफेक्ट) दिए गए रेडियोथेरेपी की खुराक, उपचार की अवधि और उपचार किए जा रहे क्षेत्र पर निर्भर करते हैं. इलाज के इरादे से कीमोरेडियोथेरेपी और रेडियोथेरेपी वाले मरीजों में अनुषंगी प्रभाव अधिक होगा क्योंकि रेडियोथेरेपी की खुराक अधिक होगी.
ग्रासनली रेडियोथेरेपी के अनुषंगी प्रभावों (साइड इफेक्ट्स) में थकावट, मतली और उल्टी, एसिड प्रतिवाह और सीने में जलन, गले में खराश और निगलने में कठिनाई, सख्ती (ग्रासनली का संकुचित होना), खांसी और बेहोशी शामिल हैं. अनुषंगी प्रभाव तीव्र हो सकते हैं, जहां वे उपचार के दौरान और तुरंत बाद होते हैं या जब उपचार के 3 महीने से अधिक समय बाद होते हैं. उपचार के पूरा होने के बाद तीव्र अनुषंगी प्रभावों में लगभग 4 सप्ताह लगते हैं.
निगलने में कठिनाई का प्रबंध करना
निगलने में कठिनाई रखने वाले और पर्याप्त आहार नहीं ले पा रहे मरीजों में एक फीडिंग ट्यूब लगायी जा सकती है ताकि मरीज को उपचार प्राप्त करने और उससे उबरने के दौरान उसकी जरूरत का सारा पोषण मिल सके. यह फीडिंग ट्यूब एक फीडिंग जेन्जोस्टॉमी हो सकती है जहां ट्यूब को छोटी आंत में रखा जाता है जिसे जेजुनम या गैस्ट्रोस्टोमी कहा जाता है, जहां ट्यूब को पेट में रखा जाता है. ये ट्यूब त्वचा से निकलती हैं और भोजन और तरल पदार्थ ट्यूब के माध्यम से अंदर डाले जा सकते हैं.
पेम्ब्रोलीज़ुमैब के साथ इम्यूनोथेरपी का उपयोग उन मरीजों में किया जा सकता है जो पीडी-एल 1 पॉजिटिव हैं या जिनमें माइक्रोसेटेलाइट अस्थिरता (एमएसआई) का उच्च स्तर है, और जिन्हें बहुत उन्नत या मेटास्टेटिक एसोफैगियल कैंसर है। यह उपचार इस सेटिंग में सभी मरीजों के लिए उपयुक्त नहीं हो सकता है। उपर्युक्त मरीजों में कीमोथेरपी के बाद के उपचार रूप में पेम्ब्रोलीज़ुमैब का उपयोग किया जा सकता है।
वे रोगी जो कैंसर से ग्रस्त हैं और भोजन निगलने में सक्षम नहीं हैं, उनके लिए एसोफैगियल स्टेंट का इंजर्शन एक विकल्प है। स्टेंट से ग्रासनली के लुमेन को खोलने में मदद मिलती है जिससे भोजन गुजर पाता है। स्टेंट एक मेटैलिक मेश वायर होता है जिसे एंडोस्कोपी द्वारा ग्रासनली में डाला जाता है। जब यह जगह पहुँच जाता है, तो वहाँ से इसका विस्तार किया जा सकता है। स्टेंट प्लेसमेंट के दुष्प्रभावों में छाती में परेशानी, दर्द और दिल में जलन होना शामिल है।





